ACIDIFIER SEBAGAI FEED ADITIF
Oleh: Syam Rahadi
(Dosen Fakultas Peternakan, Universitas Halu Oleo, Kendari)
I. PENDAHULUAN
1.1 Latar Belakang
Usaha peternakan terus berkembang seiring dengan meningkatnya permintaan produk hewani. Bersama dengan bibit dan manajemen, pakan merupakan faktor utama dalam budidaya ternak. Misalnya biaya pakan merupakan biaya terbesar dalam bisnis unggas, sekitar 60-70% berasal dari pakan dan sisanya berasal dari biaya produksi lainnya. Untuk menurunkan biaya pakan yang tinggi, perlu dilakukan peningkatan efisiensi pemanfaatan pakan oleh unggas sehingga peningkatan pendapatan dapat tercapai, Biaya produksi dapat ditekan jika efisiensi pakan yang diberikan pada ternak meningkat. (Halim, 2008).
Dewasa ini industri unggas maupaun babi dihadapkan kepada permasalahan untuk memproduksi daging yang rendah kolesterol, rendah total lipid dan rendah asam lemak jenuh, tetapi kaya asam amino tertentu seperti asam aspartat, asam glutamat dan arginin, rendah tingkat kontaminasi oleh mikrobia patogen dan bebas residu kimia sintetik .
Pada unggas dan babi, ada beberapa cara untuk mengoptimalkan efisiensi penyerapan zat makanan di dalam saluran pencernaan. Salah satu cara yang umum digunakan oleh peternak saat dengan memanfaatkan antibiotik. Permasalahannya adalah bahwa aditif pakan komersial yang beredar di pasar selain mengandung senyawa kimia sintetik juga tidak mampu memproduksi daging dengan kriteria tersebut di atas. Pada umumnya, aditif pakan komersial disusun oleh senyawa-senyawa sintetik, yang telah dibuktikan mempunyai side effect yang tinggi seperti merusak sistem hormonal dan kekebalan tubuh (Cao dkk., 2004), menimbulkan retensi mikroba dan residu antibiotik dalam tubuh ayam sehingga membahayakan manusia yang mengkomsumsinya.
Selain permasalahan tersebut di atas, aditif pakan komersial tidak dirancang untuk dapat mengatasi stres panas pada broiler yang dipelihara pada suhu tinggi. Untuk mengatasi permasalahan tersebut, maka perlu dicarikan alternatif aditif pakan alami yang mampu meningkatkan produkstivitas dan memproduksi daging berkualitas. Aditif pakan alami tersebut harus mengandung senyawa aktif yang memberikan side effect yang lebih kecil dari pada senyawa kimia sintetik serta berpotensi untuk digunakan sebagai aditif pakan alami untuk memproduksi daging berkualitas serta mampu mengatasi stres panas pada unggas.
Mengatasi berbagai permasalahan dan kelemahan atas penggunaan aditif pakan komersial atau sintetis dalam pakan, maka perlu dicarikan alternatif aditif pakan alami yang dapat menggantikan aditif pakan komersial tersebut yang mampu memproduksi daging yang efisien. Aditif pakan alami tersebut harus mengandung senyawa aktif yang memberikan side effect yang lebih kecil dari pada senyawa kimia sintetik serta berpotensi untuk digunakan sebagai aditif pakan alami untuk memproduksi daging yang aman serta mampu mengatasi stress panas pada ayam broiler. Salah satu jenis aditif pakan yang telah lama diaplikasinkan pada ternak adalah acidifier.
Acidifier adalah aditif pakan berupa asam organik yang dapat diberikan melalui pakan atau air minum. Penambahan asam organik dapat menjaga keseimbangan mikrobia dalam saluran pencernaan dengan cara mempertahankan pH saluran pencernaan, sehingga penyerapan protein meningkat (Natsir, 2008). Aktivitas saluran pencernaan terutama usus halus yang berperan penting dalam pencernaan dan penyerapan nutrien dapat dibantu dengan pemberian acidifier.
Efek penggunaa acidifier dapat mengurangi pertumbuhan bakteri dan jamur dalam bahan pakan dan dengan demikian menjaga kualitas pakan. Acidifier jika ditambahkan dalam jumlah yang cukup mempunya dampak positifnya terhadap kesehatan dan produktifitas ternak. Asam yang digunakan sebagai aditif pakan adalah senyawa yang secara alami terjadi pada metabolisme sel, sehingga merupakan produk alami dengan toksisitas yang rendah. Pemberian acidifier dapat menurnkan konversi pakan dan meningkatkan keuntungan harian, serta penurunan kejadian diare, meningkatkan pengembalian ekonomi dengan biaya pakan yang lebih rendah dan produknya dapat dipasarkan waktu yang lebih singkat (Freiting, 2007).
1.2 Rumusan Masalah
Berdasarkan latar belakang yang telah dipaparkan yang menjadi permasalahan yang perlu dikaji adalah bagaimana mekanisme aksi acidifier dapat menurunkan pH dalam pakan/air minum dan maupun saluran pencernaan, serta bagaimana mekanisme aksi dalam intraseluler mikrobial.
1.3 Tujuan
Tujuan tulisan ini adalah:
- Mengkaji mekanisme aksi acidifier dalam saluran pencernaan terhadap penurunan pH, dan aktifitas antimikrobial;
- Mengaji dampak penggunaan acidifier terhadap metabolisme, pertumbuhan, kontrol coli dan Salmonella;
- Mengkaji faktor risiko penggunaan acidifier;
1.3 Manfaat
Manfaat yang dapat diperoleh dari kajian ini adalah :
- Sebagai bahan sumber informasi bagi peternak tentang pemanfaatan acidifier sebagai bahan aditif pakan untuk meningkatkan produktifitas ternak.
- Bagi mahasiswa dan peneliti sebagai bahan pengetahuan dalam pengembanagan penelitian lebih lanjut dalam optimalisasi acidifier sebagai aditif pakan.
II. ACIDFIER PADA NUTRISI TERNAK
2.1 Aditif Pakan Acidifier
Acidifier adalah asam yang termasuk dalam pakan untuk menurunkan pH pakan, usus, dan sitoplasma mikroba sehingga menghambat pertumbuhan mikroflora patogen. Penghambatan ini mengurangi mikroflora yang bersaing untuk nutrisi inang dan menghasilkan pertumbuhan dan kinerja yang lebih baik. Asam organik telah digunakan secara ekstensif selama lebih dari 25 tahun dalam produksi babi dan baru-baru ini di unggas. Efek antimikroba dari ion asam organik dalam mengendalikan populasi bakteri di saluran pencernaan bagian atas yang menyebabkan efek menguntungkan. Penggunaan asam anorganik seperti HCl dan H3PO4 dapat mereduksi pH tetapi tidak efektif. (Reddy, 2004).
Potensi penggunaan asam organik sebagai pakan ternak dan pengawet biji-bijian dan pakan ternak telah dikenal selama beberapa dekade dan didokumentasikan dalam banyak publikasi ilmiah. Produk sampingan alami dari fermentasi mikroba, dan juga terjadi secara alami pada tanaman, asam organik telah digunakan selama ribuan tahun sebagai pengawet makanan. Inilah menjadi salah satu sebab mengapa industri dan masyarakat umum dapat diterima dan dapat dimanfaatkan untuk mengoptimalkan produksi ternak. Acidifier teakh memberi kontribusi mendasar untuk memproduksi pakan yang higyenis, karena acidifier menekan pertumbuhan jamur dan bakteri patogen, sehingga memungkinkan penggunaan sumber pakan lebih baik. (Lückstädt, et al., 2014)
Asam organik juga merupakan pilihan dalam peningkatan kinerja peternakan untuk menghemat biaya dan rama lingkungan, hal tersebut berlaku untuk pasar di seluruh dunia. Penggunaan acidifiers Uni Eropa telah menetapkan standar Eropa dan diharapkan dapat dilakukan di tempat lain secara global, untuk ternak babi, unggas dan akuakultur, untuk pengawetan biji-bijian, dan dalam menangani masalah makanan dan pakan. Asam organik semakin mendapatkan penerimaan seluruh dunia dalam industri nutrisi ternak (Lückstädt, et al., 2014)
Sebagai kelompok bahan kimia, asam organik dianggap sebagai asam karboksilat organik, termasuk asam lemak dan asam amino, dengan struktur umum R-COOH. Asam organik yang umum dan struktur dan sifat kimianya ditunjukkan pada Tabel 1.
Tabel 1. Sifat Fisiko Kimia Asam Organik
|
Asam Lemak |
Formula MolekulerA |
pKa |
Kelarutan dalam air |
Berat molekul (g/mol) |
Density (g/ml) |
Kondisi Fisik |
|
Formik |
HCOOH |
3,75 |
∞ |
46,03 |
122 |
cair |
|
Asetat |
CH3COOH |
4,76 |
∞ |
60,05 |
1049 |
cair |
|
Propionat |
CH3CH2COOH |
4,88 |
∞ |
74,04 |
0993 |
cair |
|
Butirat |
CH3CH2CH2COOH |
4,82 |
∞ |
88,12 |
0958 |
cair |
|
Laktat |
CH3CH(OH)COOH |
3,83 |
v |
90,08 |
1206 |
cair |
|
Sorbik |
CH3CH:CHCH:CHCOOH |
4,76 |
s |
112,14 |
1204 |
cair |
|
Fumarik |
COOHCH:CHCOOH |
3,02 4,38 |
s |
116,07 |
1635 |
cair |
|
Malik |
COOHCH2CH(OH)COOH |
3,4 5,1 |
∞ |
134,09 |
|
cair |
|
Tartarik |
COOHCH(OH)CH(OH)COOH |
2,93 4,23 |
v |
150,09 |
176 |
cair |
|
Sitrat |
COOHCH2C(OH)(COOH)CH2COOH |
3,13 4,76 6,4 |
v |
192,14 |
1665 |
padat |
Sumber: Foegeding dan Busta (1991) dalam Parten dan Mroz (1999)
Keterangan: ∞: larut dalam tinggi ; v: kelarutan sedang ; s: kelarutan rendah
Asam format
Asam format adalah cairan transparan yang tidak berwarna dan berbau tajam. Hal ini biasa digunakan sebagai bahan pengawet dalam memilah pakan ternak dan berbagai produk sampingan yang mengandung sedikit substrat untuk produksi asam laktat yang diinginkan oleh lactobacilli. Formate adalah penyusun alami jaringan hewan dan darah. Secara metabolik penting dalam transfer zat perantara 1-C yang dihasilkan terutama selama metabolisme asam amino, dan berfungsi sebagai substrat untuk biosintesis pangkalan purin dan dengan demikian asam nukleat (Stryer, 1988 dalam Parten dan Mroz, 1999).
Asam asetat, propionat dan asam butirat
Asam asetat adalah cairan yang tidak berwarna dengan bau yang menyengat. Ini dihasilkan melalui oksidasi alkohol oleh bakteri Acetobacter. Asam propionat dan n-butirat keduanya adalah cairan berminyak dan memiliki bau tengik yang tidak menyenangkan. Asam propionat diproduksi oleh Propionibacterium dalam pembuatan keju (Foegeding & Busta, 1991; dalam Parten dan Mroz, 1999).
Asam laktat
Asam laktat diproduksi oleh banyak spesies bakteri, terutama genera Lactobacillus, Bifidobacterium, Streptococcus, Pediococcus dan Leuconostoc. Ini adalah penyusun alami beberapa bahan makanan dan merupakan salah satu bahan pengawet tertua. Tindakan antimikroba asam laktat diarahkan terutama terhadap bakteri, sedangkan banyak jamur dan ragi dapat memetabolismenya (Foegeding & Busta, 1991; dalam Parten dan Mroz, 1999).
Asam sitrat dan fumarat
Asam sitrat dan fumarat keduanya bersifat kristalin dan tidak berbau. Asam sitrat memiliki rasa asam yang menyenangkan dan asam fumarat memiliki asam amino. Asam sitrat umumnya merupakan agen antimikroba yang kurang efektif dibandingkan asam organik lainnya, sebagian karena banyak mikroorganisme dapat memetabolisme dan juga karena pKa yang rendah (Foegeding & Busta, 1991, rendah. dalam Parten dan Mroz, 1999).
2.2 Mekanisme Aksi Acidifier
2.2.1 Aplikasi pada air minum
Air adalah nutrisi yang paling penting bagi ternak. Ternak biasanya menelan setidaknya dua kali lebih banyak air dari pakan. Pada suhu lingkungan yang lebih tinggi, konsumsi air dapat meningkat lebih banyak. Ternak dengan kinerja tinggi dalam produksi ternak modern semakin kurang toleran terhadap stresor seperti kualitas air yang buruk. Penerapan asam organik ke air minum dapat memberikan solusi untuk efek negatif kualitas air yang rendah terhadap kesehatan dan kinerja ternak. Penggunaan asam organik dalam air dapat mengendalikan mikroorganisme yang tidak diinginkan dengan mengurangi pH, serta melalui aktivitas langsung pada mikroorganisme. pH berkurang oleh pelepasan proton asam (H+) ke dalam air. Setiap asam organik memiliki karakteristi fisik dan kimia tersendiri, yang mengarah ke aktivitas antimikroba tertentu. Saat mengaplikasikan single acid ke air, pH akan menurun dengan cepat, karena pelepasan secara cepat proton. Asam buffer memiliki efek yang lebih lemah terhadap reduksi pH. Asam yang disangga adalah asam yang dicampur dengan basa konjugasi. Basa konjugasi dalam campuran neutron ini melepaskan proton, oleh karena itu reduksi pH akan kurang dibandingkan dengan single acid. Data internal menunjukkan bahwa asam buffer menghasilkan pH akhir yang lebih tinggi dari larutan daripada bila asam unbuffered digunakan. (Lückstädt, et al., 2014).
2.2.2 Dampak pada Pakan
Dalam kondisi baik, semua pakan komplit memiliki kandungan, bakteri dan jamur tertentu, dan bisa dibayangkan berapa kali jumlahnya dalam kondisi penyimpanan yang tidak menguntungkan. Bahan pengawet dapat mengurangi kejadian kontaminasi mikroba dalam pakan dan dengan demikian jumlah kuman dikonsumsi oleh ternak berkurang dan kualitas pakan meningkat secara signifikan. Penambahan asam organik dalam pakan menurunkan nilai pH pakan dan juga memberikan kapasitas pengikat asam. Terutama untuk anak babi, efek menguntungkan dari penggunaan asam. Pada saat penyapihan, pencernaan enzimatik maupun produksi asam hidroklorida di perut anak babi cukup berkembang. Selain itu, selama periode starter pakan yang digunakan dengan kapasitas pengikatan asam tinggi karena mengandung protein kasar dan makro yang tinggi. Dengan komposisi pakan yang spesifik ini yang mengandung asam organik, dapat mengurangi stres yang umum terjadi pada anak babi karena pemisahan dari induk babi. Selama periode penyapihan semua faktor ini dapat menyebabkan risiko masalah kecernaan dan diare lebih tinggi (Schöner, 2001).
2.2.3 Efek dalam saluran pencernaan
Pengaruh asam organik dalam saluran pencernaan dapat dibagi menjadi dua bagian, pengasaman dan aksi anion asam organik. Penambahan asam organik menginduksi reduksi nilai pH yang lebih cepat di dalam saluran pencernaan, yang berakibat pada waktu yang lebih singkat untuk mencapai pH optimum 4 sampai 3.
Kisaran pH ini diperlukan untuk aktivasi pepsinogen dan pepsin yang optimal. Respon tersebut menyebabkan peningkatan kecernaan protein, yang telah terbukti beberapa kali (Gambar 1).
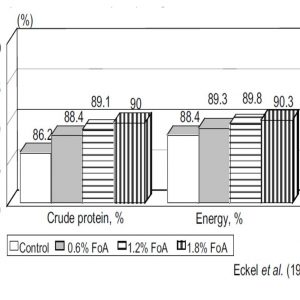
Gambar 1. Pengaruh asam format (FoA) terhadap kecernaan protein dan energi pada anak babi (5-12 kg LW).
Sumber: Eckel et al. (1992) dalam (Schöner, 2001)
Penambahan asam format mengurangi pembentukan amonia di lambung anak babi, yang mungkin disebabkan oleh pengurangan deaminasi asam amino. Akibatnya, lebih banyak asam amino diserapa dan retensi protein. Pengurangan pH yang dipercepat di dalam lambung juga memiliki efek menghambat mikroorganisme dengan toleransi asam rendah di lambung. Namun, efek pada mikroflora pada duodenum anak babi tampaknya terutama disebabkan oleh penambahan anion. Dalam percobaan ini, Kirchgessner dkk. (1992) memperoleh reduksi yang hampir sama dengan E. coli, Enterococci dan Bacteriodaceae ketika formate kalsium atau asam format (dalam bentuk dosis setara) digunakan (Schöner, 2001).
2.2.4 Mekanisme Penurunan pH
Air adalah nutrisi yang paling penting bagi ternak. Hewan biasanya menelan setidaknya dua kali lebih banyak air sebagai pakan. Pada suhu lingkungan yang lebih tinggi, asupan air dapat meningkat lebih lanjut. Hewan dengan kinerja tinggi dalam produksi hewan modern semakin kurang toleran terhadap stresor seperti kualitas air yang buruk. Penerapan asam organik ke air minum dapat memberikan solusi untuk efek negatif kualitas air yang rendah terhadap kesehatan dan kinerja hewan ternak.
Penggunaan asam organik dalam air mengendalikan mikroorganisme yang tidak diinginkan dengan mengurangi pH, serta melalui aktivitas langsung pada mikroorganisme. PH berkurang oleh proton pelepasan asam (H +) ke dalam air. Setiap asam organik memiliki karakteristik fisik dan kimia tersendiri, yang mengarah ke aktivitas antimikroba tertentu. Saat menerapkan asam tunggal ke air, pH akan menurun dengan cepat, karena pelepasan cepat proton. Asam penyangga memiliki efek yang lebih lemah terhadap reduksi pH. Asam yang disangga adalah asam yang dicampur dengan basa konjugasi. Basa konjugasi dalam campuran neutron ini melepaskan proton, oleh karena itu reduksi pH akan kurang dibandingkan dengan asam tunggal. Data internal menunjukkan bahwa asam buffer menghasilkan pH akhir yang lebih tinggi dari larutan dari pada bila hanya asam unbuffered yang digunakan. Hal ini penting dalam pengasaman air minum, karena bila pH airnya terlalu rendah, konsums airnya bisa berkurang. Selain itu, dosis asam organik yang cukup dapat ditambahkan ke air untuk pengawetan sambil membatasi reduksi pH air. Oleh karena itu, menggunakan campuran sinergis dari asam bebas dan buffer adalah strategi yang paling menguntungkan untuk kemanjuran produk. (Van Immerseel, 2009).
2.2.5 Aktifitas antibakteri
Dalam banyak aplikasi, efisiensi asam organik ditentukan oleh mode aksi yang sama. Ini terutama didasarkan pada efek antimikroba dari asam organik pada mikroorganisme dan efek menguntungkan yang dipicunya. Cara kerja asam organik nampaknya sama, terlepas dari asam yang digunakan dan mikroorganisme yang terpengaruh. Asam organik adalah asam lemah, yang berarti bahwa proporsi molekul tertentu tetap tidak terdisosiasi, bergantung pada nilai pKa asam dan tingkat pH sekitar. Molekul tak beraturan yang tidak terkoordinasi ini melewati membran sel ke mikroorganisme dengan lebih mudah. Begitu berada di dalam sel mikroba, asam melepaskan protonnya (H+) di lingkungan alkalin yang lebih basa dari sitoplasma, sehingga terjadi penurunan pH intraselular bakteri. Ini mempengaruhi metabolisme mikroba, menghambat aksi enzim penting mikroba. Sel bakteri dipaksa mengeluarkan energi untuk mengeluarkan proton, yang menyebabkan akumulasi anion asam intraselular, tergantung pada gradien pH di seluruh membran. Anion di dalam sel mikroba diperkirakan mengganggu proses metabolisme dalam sel, termasuk sintesis RNA dan DNA. Hal ini menyebabkan kelipatan sel dan membatasi pertumbuhan. Beberapa penyelidikan telah menunjukkan efek bakterisida yang kuat dari asam organik tanpa menurunkan pH dalam saluran GI/gastrointestinal secara signifikan, memberikan bukti untuk mode tindakan yang dijelaskan di atas. Akibatnya, asam organik masih bisa menunjukkan khasiat lebih kuat dibandingkan dengan asam inorganic (yang hanya mengurangi pH dan tidak bisa masuk sel) (Lückstädt, et al, 2014)
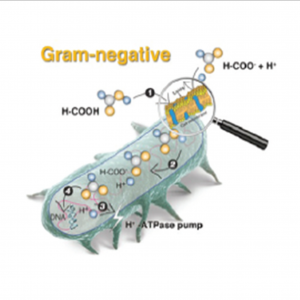 Gambar 2. Cara kerja asam organik terhadap bakteri gram negative
Gambar 2. Cara kerja asam organik terhadap bakteri gram negative
(Sumber: Lückstädt, 2014)
Keterangan:
- Asam organik yang tidak terdisosiasi masuk ke sel bakteri.
- Disosiasi proton, menyebabkan reduksi pH.
- Pengusiran proton dengan proses menuntut energi.
- Efek penghambatan anion asam pada DNA.
Selain itu, acidifiers dapat memiliki efek pemberantasan awal pada bakteri dalam pakan dan tetap berada di sana sebagai penghalang pertama, mencegah kontaminasi kembali. Bahkan dalam kondisi yang baik, semua pakan majemuk memiliki kandungan kuman (bakteri, virus, jamur dan protozoa) tertentu, yang mungkin berkembang biak dalam kondisi panen dan penyimpanan yang tidak menguntungkan (Schöner, 2001). Pengawet mengurangi kejadian kuman dalam pakan dan dengan demikian jumlah kuman dikonsumsi oleh ternak. Kualitas pakan meningkat secara signifikan, penambahan asam organik menurunkan nilai pH pakan dan juga memberikan kapasitas pengikat asam.
Sebenarnya, asam organik yang terkait dengan aktivitas antimikroba tertentu adalah asam rantai pendek (SCFA, C1-C7) dan merupakan asam monokarboksilat sederhana seperti asam format, asetat, propionat dan asam butirat, atau asam karboksilat, yang memiliki gugus hidroksil (biasanya pada karbon) seperti asam laktat, malat, asam tartarat, dan sitrat. Empat asam organik yang biasa digunakan dalam asam pakan – formik, asetat, propionat dan asam laktat – memiliki kemampuan spesifik untuk menembus dinding sel bakteri dan membunuh bakteri dengan mengganggu metabolisme mereka. Asam ini hanya melewati membran dalam bentuk yang tidak terdisosiasi. Tindakan antimikroba utama mereka (penghambatan atau penundaan pertumbuhan selektif) adalah melalui depresi pH diet. Namun, kemampuan asam organik untuk berganti dari bentuk yang tidak terikat ke bentuk yang dipisahkan, tergantung pada pH lingkungan, menjadikannya zat antimikroba efektif. Bila asam berada dalam bentuk yang tidak terdisosiasi, dapat dengan bebas menyebar melalui membran semi permeabel mikroorganisme ke dalam sitoplasma sel mereka. Begitu berada di dalam sel, di mana pH dipertahankan mendekati 7, asam tersebut memisahkan dan menekan enzim sel (dekarboksilase dan katalase) dan nutrisi. sistem transportasi (Lueck, 1980 dalam Papatsiros dan Bilinis 2014).
Khasiat asam dalam menghambat mikroba bergantung pada nilai pKa-nya dimana pH di mana 50% asam terdisosiasi. Asam organik dengan nilai pKa lebih tinggi adalah pengawet yang lebih efektif dan khasiat antimikrobanya umumnya meningkat dengan meningkatnya panjang rantai dan tingkat unsaturation (Foegeding & Busta, 1991).
Dalam prakteknya ini berarti pH lambung harus lebih rendah dari 5 untuk hasil yang optimal. Tanpa asam antimikroba spesifik ini, pH harus sangat rendah untuk menghancurkan bakteri. Beberapa garam asam di atas, juga terbukti memiliki manfaat pada kinerja pertumbuhan. Asam lain, seperti asam sorbat dan fumarat, memiliki beberapa aktivitas antijamur dan merupakan asam rantai-karboksilat pendek, yang mengandung ikatan rangkap. Asam organik adalah asam lemah dan hanya sebagian terpisah; Kebanyakan dari mereka, dengan aktivitas antimikroba, memiliki pKa 3 – 5 (Papatsiros dan Billinis, 2014)
Selain itu, masing-masing asam memiliki spektrum aktivitas antimikroba tersendiri. Efek antimikroba mereka bervariasi dari satu asam ke asam lain, bergantung pada konsentrasi dan pH (Chaveerach et al., 2002). Sebagai contoh, asam laktat lebih efektif dalam mengurangi pH lambung dan koliform (Tsiloyiannis; et al, 2001) sedangkan asam lain, seperti formik, propionik memiliki aktivitas antimikroba lebih luas dan dapat efektif terhadap bakteri (misalnya koliform, clostridia, Salmonella), jamur dan ragi (Øverland et al. 2008).
Senyawa asam yang digunakan sebagai bahan tambahan pakan adalah rantai pendek dan rantai asam lemak menengah. Seperti telah disebutkan di atas, konsep asli untuk menggabungkan asam ini ke dalam pakan didasarkan pada pendapat bahwa asam akan mendekontaminasi makanan itu sendiri dan mencegah Salmonella pada ayam. Selanjutnya, disadari bahwa penambahan asam in-feed juga memberi efek pada tanaman dan saluran gastro-intestinal ternak tersebut. Sejumlah penelitian telah dilakukan dengan menggunakan berbagai asam organik yang ditambahkan pada pakan atau air minum, pada model infeksi dimana serotipe Salmonella yang berbeda digunakan untuk inokulasi langsung pada tanaman atau inokulasi umpan (Van Immerseel, 2009)
2.2.6 Dampak pada metabolism dan pertumbuhan
Efek menguntungkan dari asam organik dan garamnya terhadap kinerja pertumbuhan telah dikonfirmasi dalam beberapa penelitian. Asam amino yang ditambahkan pada makanan babi berpotensi membantu memperbaiki kinerja pertumbuhan dengan memperbaiki proses pencernaan melalui beberapa mekanisme. Dipercaya bahwa acidifiers dapat meningkatkan kinerja pertumbuhan dengan: (Papatsiros dan Billinis, 2014)
- Meningkatkan kesehatan usus dengan mempromosikan pertumbuhan bakteri yang menguntungkan, sekaligus menghambat pertumbuhan mikroba patogen (melalui pengurangan pH dan kapasitas buffer makanan). Kapasitas buffering yang berkurang dari makanan yang mengandung asam organik juga diharapkan dapat memperlambat perkembangan dan / atau kolonisasi mikroba yang tidak diinginkan, mis. E. coli, clostridia di daerah gastro-ileal (jejunum, cecum) (Partanen & Mroz, 1999). Selain itu, asam organik atau garamnya tidak dapat memperbaiki kinerja pertumbuhan hewan, namun secara tidak langsung dapat meningkatkan pH sekum dan konsentrasi amonia sekum (Biagi et al 2007).
- Merangsang – memperbaiki sekresi pancreas, yang meningkatkan daya cerna, penyerapan dan retensi protein dan asam amino (Blank et al, 1999) dan mineral (seperti Ca, P, Mg dan Zn – terutama Ca dan P) (Valencia and Chavez, 2002) dalam makanan. Umumnya dianggap bahwa asam organik pakan menurunkan pH lambung, sehingga meningkatkan aktivitas enzim proteolitik dan waktu retensi lambung.
- Mempengaruhi morfologi usus dengan mempromosikan perubahan fungsi pencernaan dan saya, asam organik bekerja secara positif pada pertumbuhan mikroba dan produksi amonia oleh mikroflora sekum pigmen. Biagi dan Piva (2007) melihat bahwa berbagai asam (formik, asetat, propionat, laktat, mentega, sorbik, fumarat, malat, sitrat, benzoat) dapat menghambat atau meningkatkan aktivitas bakteri pada sekum dan secara positif dapat mempengaruhi mikroflora sekum secara in vitro. mengurangi konsentrasi amonia. Telah diketahui dengan baik bahwa asam lemak rantai pendek (asam asetat, propionat dan n-butirat) yang dihasilkan oleh fermentasi mikroba karbohidrat merangsang proliferasi sel epitel (Sakata et al 1995) dan kekuatan efek asam organik adalah sebagai berikut: n -butyric> propionic> asam asetat (Sakata, 1987).
Efek komparatif asam laktat dalam cairan dan encapsulated dari pada mikroflora usus dirangkum dalam Tabel 4. Bentuk asam laktat hanya secara signifikan mengurangi (p, 0,01)) jumlah salmonella sp, bila berada dalam makanan. Tingkat rendah ini tidak bentuk yang terenkapsulasi. Fakta ini mungkin terkait dengan pH yang dicapai saat bentuk asam laktat yang dienkapsulasi ditambahkan. Level asam laktat seca signifikan meningkatkan julam Bakteri asam laktat, tetapi tidak mempengaruhi jumlah E. coli. Tingkat rendah E. coli ini tidak tercapai bila bentuk encapsulated asam laktat ditambahkan dalam makanan. Jumlah Lactobacillus dan Salmonella sp tidak dipengaruhi oleh tingkat asam laktat. Gunal (2006) melaporkan adanya penurunan bakteri total dan bakteri gram negatif yang ditemukan di usus halus. Dalam pandangan mikroflora usus, penggunaan. Asam laktat yang dienkapsulasi dalam makanan lebih disukai karena kemampuannya untuk menghasilkan jumlah bakteri asam laktat tertinggi dan jumlah terendah Salmonell sp. Disimpulkan bahwa penggunaan. Asam laktat yang dienkapsulasi meningkatkan kinerja broiler, pH usus lebih rendah dan meningkatkan panjang villi dan mengurangi jumlah Salmonella sp. (Natsir, et al., 2010)
2.3 Faktor Risiko Penggunaan Acidifier
- Asam dapat memiliki efek negatif pada palatabilitas diet, saat ditambahkan pada asam tingkat yang berlebihan, menghasilkan asupan pakan yang lebih rendah atau penolakan makan (Partanen & Mroz, 1999).
- Asam pada tingkat tinggi dalam umpan bersifat korosif terhadap semen dan baja galvanis pada rumahan babi, sehingga menimbulkan penanganan dan masalah peralatan ke produsen pakan. Sebagai contoh, asam format adalah yang paling korosif untuk peralatan dan berbahaya untuk ditangani, sementara asam fumuric mudah ditangani (Mateos et al., 1999 dalam Papatsiors dan Billinis 2014). Garam asam organik umumnya tidak berbau dan kurang korosif dari pada bentuk asamnya, sehingga lebih mudah ditangani dalam proses pembuatan pakan (Jacela et al., 2009).
- Penggunaan asam organik dalam bentuk bebas, dari pada tingkat yang telah terbukti berkhasiat, dapat menyebabkan masalah palatabilitas (Partanen & Mroz, 1999)), merusak mukosa perut dan duodenum (Argenzio & Eisemann, 1996), serta menyebabkan demineralisasi tulang (Partanen & Mroz, 1999) dan stres asam, menginduksi resistensi mekanisme terhadap asam organik pada bakteri tertentu (Bearson et al 1997).
Upaya meminimalkan efek negated dalam penggunan asam organik harus dievaluasi untuk menentukan jumlah minimum jumlah asala organic yang efektif yang akan digunakan Strategi lain untuk memperpanjang efektivitas suplemen asam organik dan mengurangi kerusakan korosi pada kandang yaitu penggunaan asam organik dengan pelepasan asam yang lambat.
III. PENUTUP
3.1 Kesimpulan
- Asam organik bisa dibilang aditif pakan paling efektif & ramah lingkungan.
- Aplikasi penggunaan asam organik dapat diberikan dengan cara dismeprotkan langsung kepakan, dicampurkan pakan dan pemiks, dan melalui air minum.
- Penggunaan asam organik dapat menurunkan pH pakan, pH air minum dan pH saluran pencernaan dan dapat menghamt patogen yang berbahaya.
- pemberian asam organik dapat melawan secara efektif mikrobial coli dan Salmonella.
- Asam organik meningkatkan kecernaan protein dan energi dengan mengurangi kompetisi mikroba dengan inang.
- Effect asam organik melampaui antibiotik, termasuk pengurangan BC, peningkatan sekresi pankreas, dan efek pada mukosa.
3.2 Saran
Perlu dilakuan penelitian dan diaplikasikan dalam pemeliharaan ternak, terutama pada unggas dan babi untuk mengurahi penggunaan antibiotik yang telah terbukti mempunyai side effek yang berbahaya pada ternak maupun manusia.
DAFTAR PUSTAKA
Berason, S., B. Bearson, and J.W. Foster. 1997. Acid stress responses in enterobacteria. FEMS Microbilogy Letter, 147:173-180.
Blank, R., W. C. Sauer, R. Mosenthin, J. Zentek, S. Huang, and S. Roth. 1999. Effect of fumaric acid supplementation and dietary buffering capacity on the concentration of microbial metabolites in ileal digesta of young pigs. Journal of Animal Science, 77(11):2974 -2984.
Biagi, G., A. Piva, M. Moschini, E. Vezzali, & F.Roth. (2007). Performance, intestinal microflora, and wall morphology of weanling pigs fed sodium butyrate. Journal of Animal Science, Vol. 85, No. 5, pp. 1184-1191
Chaveerach, P., D. A. Keuzenkamp, H.A.P. Urlings, L.J A. Lipman, and F. van Knapen. 2001. In Vitro Study on the Effect of Organic Acids on Campylobacter jejuni/coli Populations in Mixtures of Water and Feed. Poultry Science 81:621-628.
Freitag, M. 2007, Organic acids and salts promote performance and health in animal husbandry, in Acidifiers in Animal Nutrition. Editor C. Lückstädt. Nottinghm University Press. Nottinghm.
Jacela, J.Y., J.M. DeRouchey, M.D. Tokach, R.D. Goodband, J.L. Nelssen, D. G. Renter, and S.S. Dritz. 2009. Feed additives for swine: Fact sheets-acidifi ers and Antibiotics. Journal of Swine Health and Production, 17(5):270-275.
Lückstädt, C., L. Wylie, R. Remmer, R. de Kok, H.R. Costa, M. Brebels, S. Flanca, H. van Dam, M. Kinjet, Y van der Horst, S. Orkala, and C. van Heusden. 2014. Organic Acids in Animal Nutrition. Fefana. Belgium.
Partanen, K.H. and Z. Mroz. 1999. Organic acids for performance enhancement in pig diets. Nutrition Research Review, 12:117-145.
Nasir, M.H. 2008. Pengaruh Penggunaan Beberapa Jenis Enkapsulan pada Asam Laktat Terenkapsulasi sebagai Acidifier Terhadap Daya Cerna Protein dan Energi Metabolis Ayam Pedaging. J.Ternak Tropika, 6(2):13-17.
Nasir, M.H., O. Sjofjan, K. Umam, A. Manaf, and W. Widodo. 2010. Effects of Liquid and Encapsulated Lactic Acid in Broiler Diets on Performances, Intestinal Characteristics and Intestinal Microflora. J. Poult. Sci., 47:240-243.
Øverland, M. N.P. Kjos, M. Borg, E. Skjerv, and H. Sørum. 2008. Organic acids in diets for entire male pigs: Effect on skatole level, microbiota in digesta, and growth performance. Livestock Science, 115:169-178.
Papatsiros, V.G. and C. Billinis. 014. The Prophylactic Use of Acidiier as Antibacterial Agent in Swine. In: Antimicrobial Agents. Editor Varaprasad Bobbarala. Published by InTech. Croatia. pp:295-310.
Reddy, V.R. 2004. The Role of Acidifier in Poultry Nutrition. Avitech Technical Bulletin. Edition Juli 2004.
Schöner, F.J. 2001. Nutritional effects of organic acids, in Feed manufacturing in the Mediteranean region, Improving safety: From feed to food. Ciheam. Zaragoza.
Tsiloyiannis, V.K., S. C. Kyriakis, J. Vlemmas, and K. Sarris. 2001. The effect of organic acids on the control of porcine post-weaning diarrhoea. Research in Veterinary Science, 70:287–293.
Van Immerseel, F., L. De Zutter, K. Houf, F. Pasmans, F. Haesebrouck, and R. Ducatelle. 2009. World’s Poultry Science Journal, 65:367-391.
Valencia, Z. and E.R. Chavez. 2002. Phytase and acetic acid supplementation in the diet of early weanedpiglets: effect on performance and apparent nutrient digestibility. Nutrition Research, 22(5):623-632.
